( MI ) انفارکتوس میوکارد به معنی انسداد کامل یکی از عروق کرونر ، ثانویه به عوامل متعددی از جمله آترواسکلروز است . این عارضه مهمترین سندرم ناشی از بیماری های عروق کرونر (CAD) است.
انفارکتوس میوکارد زمانی ایجاد می شود که :
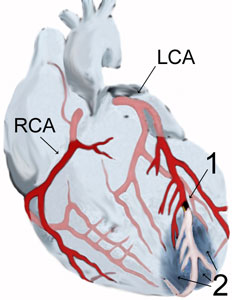
- به دنبال تنگی یا انسداد عروق کرونر ، عضله ی قلب دچار نکروز گردد .
- بدین ترتیب که پس از ایجاد انسداد در عروق کرونر ، حدود ۶ ساعت بعد در منطقه کم خونی ایجاد می شود و به علت همین کم خونی ، ناحیه رنگ پریده می شود .
- در ناحیه ایسکمیک جریان خون در عروق کند شده و یا متوقف می گردد و بدین ترتیب ترومبوز داخل عروقی پیشرفت می کند و قلب وارد مرحله صدمه بافتی یا Injury می شود که به آن مرحله ی فوق حاد انفارکتوس میوکارد گفته می شود .
- حدود ۱۸ الی ۳۶ ساعت بعد ، ناحیه ایسکمیک قرمز رنگ و سیانوزه می گردد و حدود ۴۸ ساعت بعد به رنگ خاکستری زرد در می آید .
- ۳ تا ۴ هفته بعد نیز اسکار تشکیل شده و سفید رنگ می شود .
- حدود ۶ هفته بعد ، اسکار کامل شده ، به صورت یک بافت فیبروزه عمل می کند که تقریبا در انقباضات عضله شرکت ندارد .
- مراحل فوق همگی با تغییراتی در الکتروکاردیوگرام بیمار همراه است.
![]()
علایم اصلی انفارکتوس میوکارد عبارتند از :
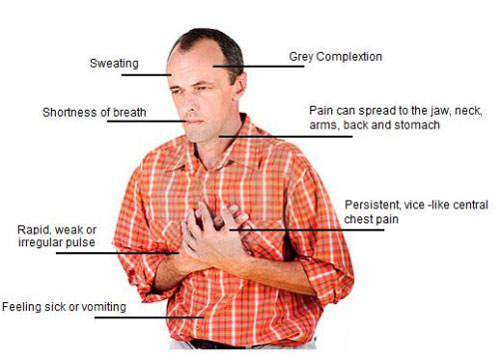
- درد قفسه سینه : درد ناشی از انفارکتوس میوکارد ، یک درد فشارنده ، سنگین و له کننده است که به طور ناگهانی بروز می کند . محل دقیق و اختصاصی این درد ، در ناحیه پشت استرنوم بوده ، به ناحیه اپیگاستر ، فک تحتانی ، بازوی چپ و پشت انتشار می یابد . این درد بیش از ۳۰ دقیقه طول می کشد و ممکن است اصلا ساکت نشود . این درد حالت پیشرونده دارد ، یعنی اول کم است و به تدریج افزایش می یابد . بنابراین یکنواخت نیست . گاهی فقط انتشار درد رخ می دهد ، مثلا بازوی چپ دچار درد می شود و در ناحیه پشت استرنوم دردی وجود ندارد .
- تعریق : همراه با درد اولیه ، تعریق رخ می دهد . انتهاهای بیمار سرد و مرطوب بوده ، عرق سرد بر پیشانی می نشیند که می تواند به دلیل تحریک سمپاتیک باشد .
- تهوع و استفراغ : تهوع معمولا در آنژین ناپایدار دیده می شود ، اما استفراغ فقط مختص انفارکتوس میوکارد است (مرکز درد و تهوع و استفراغ در مغز در نزدیکی هم قرار دارند) .
- تنگی نفس : همراه با درد ایجاد می شود و علت آن اختلال در جریان خون و افزایش فشار خون مویرگهای ریوی و احتقان ریوی است .
سایر نشانه های انفارکتوس میوکارد که احتمال بروز آنها وجود دارد عبارتند از:
- غش کردن (Faint) : وضعیتی که بیمار طی آن دچار سرگیجه و سقوط می شود ، اما از هوش نمی رود . در واقع بیمار به علت ضعف و ناتوانی قادر به صحبت نیست ، اما صداهای محیط را می شنود . در صورت وقوع بیهوشی ، به آن سنکوپ می گویند . علت بروز این عارضه ، کاهش جریان خون مغزی است که حتی ممکن است به کما بیانجامد .
- تشنج : گاهی به دنبال کاهش جریان خون مغزی ، بیمار دچار تشنج می گردد.
- سایکوز : بعضی اوقات ، بخصوص در افراد مسن ممکن است MI با علایم سایکوز همراه باشد . بنابراین اگر بیماران مسن بدون سابقه ی بیماری روانی ، با سایکوز مراجعه نمایند ، باید حتما ECG آنها کنترل شود .
- ضعف و بی حالی ناگهانی : گاهی در بیماران علایمی دال بر درد و تنگی نفس وجود ندارد . اما دچار ناتوانی ، رنگ پریدگی و کمی تعریق هستند . در چنین وضعیتی ، ECG می تواند نمایانگر MI باشد .

انفارکتوس میوکارد خاموش (Silent MI) و بدون درد (Painless MI)
SMI نوعی انفارکتوس میوکارد است که در آن بیمار فاقد علایم بالینی MI است . در حالیکه در MI بدون درد ، بیمار کلیه علایم بالینی MI را دارد و فقط فاقد درد است .
عوامل خطرزای بروز این دو نوع MI عبارتند از :
- سن بالای ۷۰ سال
- افراد سیگاری
- جنس مونث
- مبتلایان به هایپرتانسیون
وجود چند عامل خطرزا با هم ممکن است شانس بروز این نوع MI را بالا ببرد .
بررسی های اولیه از بیمار مبتلا به انفارکتوس میوکارد
- بررسی علایم حیاتی بیمار
فشار خون و نبض : مهمترین علایم حیاتی در مبتلا به MI ، کنترل فشار خون است که می تواند گویای وضعیت میوکارد باشد . به طور کلی ، هایپوتانسیون بسیار خطرناک تر از فشار خون طبیعی و یا بالا است . کمتر بودن BP از ۱۰۰mmHg و نبض کمتر از ۶۰bmp ، نمایانگر تحریک عصب واگ است که اغلب در انفارکتوس تحتانی بطن چپ رخ می دهد ، و اگر با تزریق آتروپین بهبود پیدا کند ، پیش آگهی بیمار خوب است. برادی کاردی و یا هایپوتانسیون به تنهایی ، بسیار مهم بوده ، خطرناک تلقی می شود.
ریتم قلب : بی نظمی در نبض نمایانگر وجود آریتمی بوده ، براساس نوع آریتمی موجود می تواند خطرناک باشد . نبض منظم با ریتمی برابر با ۶۰ تا ۱۰۰ ضربه در دقیقه دارای پیش آگهی خوبی است.
- تعیین کلاس فعالیت کلیپ Killip’s function class
تعیین کلاس فعالیت کلیپ براساس علایم بالینی بیمار صورت می گیرد و نمایانگر وضعیت فعلی بیمار و پیش آگهی وی است.
- Killip I :
- Killip II :
- Killip III :
- Killip IV :
- در ریه بیمار صدای اضافی شنیده نمی شود.
- گالوپ S3 وجود ندارد.
- پیش آگهی بیمار خوب بوده
- مورتالیتی کمتر از ۵% است.
- صدای گالوپ S3 در قلب و یا رال مرطوب در قواعد ریه شنیده می شود.
- میزان مورتالیتی حدود ۲۵% است.
- صدای گالوپ S3 وجود دارد
- در بیش از نیمی از ریه رال مرطوب شنیده می شود.
- میزان مورتالیتی بین ۵۰% تا ۶۰% است.
- بیمار علایم شوک کاردیوژنیک (فشار سیستولیک کمتر از ۹۰mmHg و اختلال پرفیوژن خون در تمام بدن) را از خون نشان می دهد .
- میزان مورتالیتی بین ۹۰% تا ۱۰۰% است.
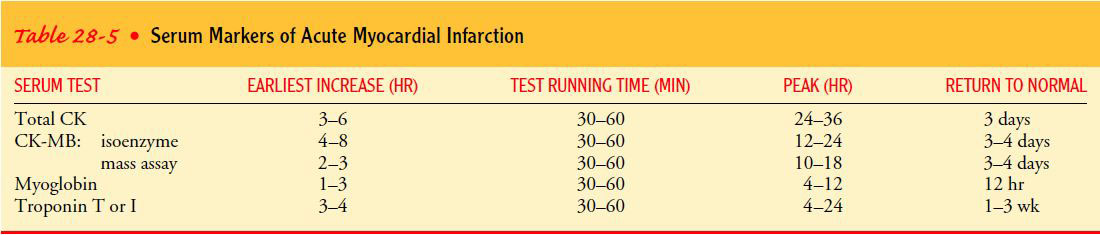
- بررسی آنزیم های قلبی
زمانی می توان گفت که بیمار دچار انفارکتوس میوکارد شده است که تغییرات الکتروکاردیوگرافیک با تغییرات آنزیمی همراه باشد. این آنزیم ها پروتئین هایی هستند که از بافت های مرده آزاد می شوند ، بنابراین حالت اختصاصی ندارند . اما بعضی از ایزو آنزیم های آنها اختصاصا مربوط به مرگ عضله ی قلبی هستند.
- کراتین فسفوکیناز (CPK) : حساس ترین و اولین آنزیمی است که پس از انفارکتوس میوکارد افزایش می یابد . دارای سه ایزو آنزیم است : CK-MM که از سلولهای نکروزه ی عضله مخطط آزاد می شود ؛ CK-BB که از سلول های مرده ی مغز خارج می شود ؛ و CK-MB که از سلول های انفارکته عضله قلب به درون خون می ریزد .
به طور کلی آنزیم CPK بعد از ۸-۴ ساعت از بروز انفارکتوس در خون آزاد می شود و مقدار آن در مدت ۲۴-۱۲ ساعت به حداکثر خود می رسد (تا ۸ برابر مقدار طبیعی). معمولا CPK بعد از ۴-۳ روز به حد طبیعی خود باز می گردد.
اما CPK-MB ، در کمتر از یک ساعت (۲۰ تا ۳۰ دقیقه) بعد از MI افزایش یافته ، بعد از سه روز به میزان طبیعی خود باز می گردد.
- تروپونین Troponin و میوگلوبین Myoglobin : این دو آنزیم دیرتر از CPK-MB در خون بالا می روند ، اما اختصاصا مربوط به قلب هستند . مقدار آنها حدودا ۳ ساعت بعد از MI افزایش یافته و طی ۲۴ ساعت به حداکثر می رسد . و سه روز بعد به حد طبیعی باز می گردد.
- سرم گلوتامیک اگزالواستیک ترانس آمیناز (SGOT) : این آنزیم در اثر تخریب سلول های عضله قلب ، عضله مخطط ، مغز ، کبد ، کلیه ،گلبول قرمز ، پانکراس و طحال آزاد می شود . میزان آن پس از انفارکتوس میوکارد ، در مدت ۱۲ الی ۲۴ ساعت به حداکثر خود می رسد و بعد از ۲ الی ۷ روز مجددا به حد طبیعی خود باز می گردد.
- لاکتات دهیدروژناز هورمون (LDH) : این آنزیم از تخریب سلول های قلب ، گلبول قرمز ، کلیه ، ریه ، مغز ، طحال و پانکراس آزاد می شود و دارای ۵ ایزوآنزیم است که دو ایزوآنزیم LDH1 و LDH2 اختصاصا در آسیب سلول های قلب افزایش می یابند . این آنزیم حدودا ۱۲ الی ۴۸ ساعت بعد از MI به داخل خون ریخته ، در مدت ۷۲ الی ۱۴۴ ساعت بعد به حداکثر مقدار خود می رسد. معمولا بعد از ۱۲-۸ روز میزان آن به حد طبیعی خود باز می گردد.
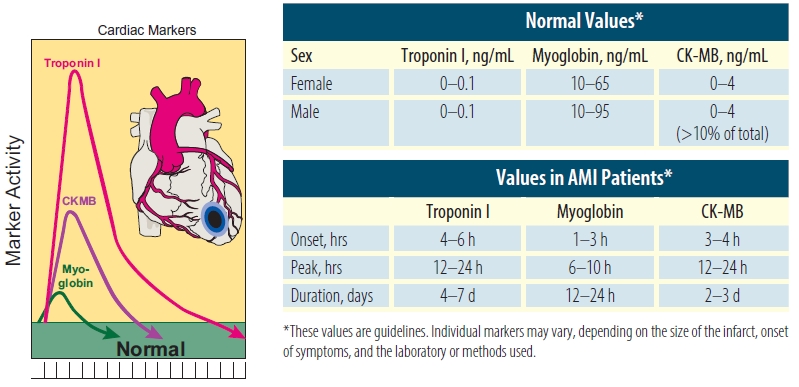
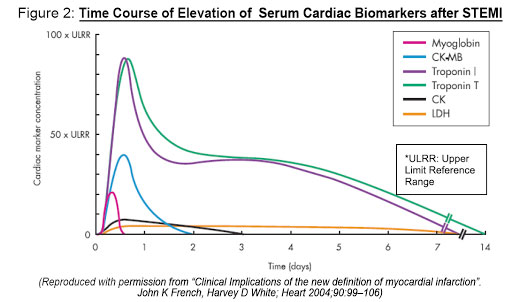
توسط رسم منحنی مربوط به تغییرات CPK می توان میزان نکروز عضله میوکارد را حدس زد. بدین منظور باید مقدار CPK را در چند روز متوالی روی منحنی رسم نمود و به سطح زیر آن توجه کرد. هر چه سطح زیر منحنی بیشتر باشد، نمایانگر افزایش سطح نکروز است. برای مثال در صورت تجویز استرپتوکیناز، پیک CPK بالا می رود، اما خیلی زود به حد طبیعی بر می گردد. آنزیم های قلبی را باید در بدو ورود ، ۱۲ ساعت، ۲۴ ساعت، و ۴۸ ساعت بعد، یعنی ۴ بار کنترل نمود.
- تغییرات CBC در حضور MI:
معمولا وجود WBC و ESR بالا همراه با تب (حداکثر ۵/۳۸) در روز سوم بعد از MI ، دلیل بر وجود التهاب است . این تغییرات ممکن است تا ۵ الی ۷ روز باقی بماند . در صورت تداوم وضعیت فوق ، مسئله عفونت مطرح می گردد.
- تغییرات WBC و ESR بعد از MI :
۴۸ ساعت بعد از وقوع MI به دلیل افزایش ترشح کاتکولامین ها ، با افزایش سطح کلسترول و تری گلیسیرید مواجه می شویم . بنابراین بعد از ۴۸ ساعت بعد از وقوع MI ، اندازه گیری لیپیدها ارزشی ندارد و این کار باید در بدو ورود بیمار انجام گیرد و اقدامات درمانی براساس آن آغاز گردد. این افزایش لیپیدی تا ۳ ماه بعد از MI باقی می ماند .
بیشترین تغییرات الکتروکاردیوگرافیک ایسکمیک میوکارد در مرحله ی رپولاریزاسیون صورت می گیرد که به صورت تغییر در قطعه ST و موج T نمایان می گردد . به طور کلی انفارکتوس میوکارد را براساس مراحل آن به سه دسته تقسیم می کنند:
- مرحله فوق حاد Hyper Acute
- مرحله حاد Acut
- مرحله مزمن Old
اما پیش از توضیح در مورد تغییرات مربوط به این مراحل ، باید به تغییرات مرحله شروع ایسکمی نیز اشاره نمود.
مرحله شروع ایسکمی
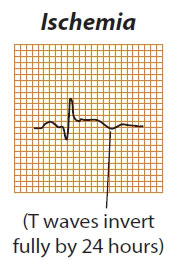 زمانی که یکی از عروق کرونر دچار مشکل می شود ، عرضه خون یا Supply به خوبی برقرار نمی گردد . معمولا علایم زمانی ظاهر می شود که بیش از ۹۰% تنگی در رگ رخ داده باشد . افرادی که کمتر از ۹۰% تنگی رگ داشته باشند معمولا در استراحت فاقد علامت هستند ، اما در هنگام فعالیت دچار درد قفسه سینه می شوند .
زمانی که یکی از عروق کرونر دچار مشکل می شود ، عرضه خون یا Supply به خوبی برقرار نمی گردد . معمولا علایم زمانی ظاهر می شود که بیش از ۹۰% تنگی در رگ رخ داده باشد . افرادی که کمتر از ۹۰% تنگی رگ داشته باشند معمولا در استراحت فاقد علامت هستند ، اما در هنگام فعالیت دچار درد قفسه سینه می شوند .
- در دقایق اول بعد از انسداد رگ ، شاهد معکوس شدن موج T هستیم .
- اما پس از ۱۰ دقیقه ، موج T شروع به مثبت شدن کرده ، قطعه ST به تدریج دچار بالارفتگی می گردد
- این علامت ورود به مرحله فوق حاد MI است.
نکته ای که در این مرحله باید به آن توجه شود ، درد قفسه سینه است . عاملی که منجر به درد قفسه سینه می شود ، ایسکمی حاد میوکارد است ، زیرا نکروز فاقد درد است . بنابراین درد علامت خطرناکی است که نمایانگر گسترش ایسکمی بوده ، هرچه مدت آن کوتاه تر باشد ، صدمه ایسکمیک کمتر است.
- مرحله فوق حاد
Hyper Acute MI
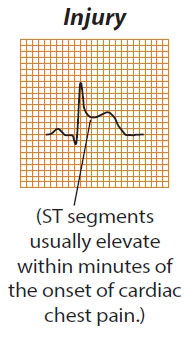 مرحله فوق حاد از شروع درد آنژینی تا ۶ ساعت بعد از آن به حساب می آید . این مرحله که وضعیت بین ایسکمی و نکروز است در واقع مرحله صدمه بافتی یا Injury بوده ، و در پایان ۶ ساعت ، انفارکتوس کامل می شود . در این مرحله، عروق کولترال فعال شده ، سعی در خونرسانی به منطقه ایسکمیک می نمایند. به این ترتیب در منطقه ای که کولترال ها از آن منشا گرفته اند ، یک ایسکمی ساب اندوکاردیال ایجاد می گردد که تغییرات مربوط به آن به صورت تغییرات متقابل یا Reciprocal در الکتروکاردیوگرام ظاهر می شود .
مرحله فوق حاد از شروع درد آنژینی تا ۶ ساعت بعد از آن به حساب می آید . این مرحله که وضعیت بین ایسکمی و نکروز است در واقع مرحله صدمه بافتی یا Injury بوده ، و در پایان ۶ ساعت ، انفارکتوس کامل می شود . در این مرحله، عروق کولترال فعال شده ، سعی در خونرسانی به منطقه ایسکمیک می نمایند. به این ترتیب در منطقه ای که کولترال ها از آن منشا گرفته اند ، یک ایسکمی ساب اندوکاردیال ایجاد می گردد که تغییرات مربوط به آن به صورت تغییرات متقابل یا Reciprocal در الکتروکاردیوگرام ظاهر می شود .
- بالا رفتگی قطعه ST : قطعه ST به میزان بیش از ۴-۳ میلی متر از خط ایزومتریک بالا می رود . باید به شکل این بالا رفتگی توجه شود . زمانی این بالا رفتگی اهمیت پیدا می کند که انحنای آن به سمت بالا باشد . در صورتی که انحنای ST به سمت پایین باشد ، دلیل بر MI نیست.
- موج T مثبت یا upright : در حضور صدمه ، موج T بلند و نوک تیز و پهن می گردد . و این علامت مهمی برای تشخیص MI در مرحله فوق حاد است.
- افزایش ولتاژ موج R : این اختلال به دلیل آهسته شدن پیشرفت جریان الکتریکی در سلول های آسیب دیده ایجاد می شود.
- افزایش زمان فعال شدن بطنی : به دلیل آهسته شدن هدایت جریان الکتریکی در سلول های آسیب دیده ، زمان فعال شدن بطنی یا VAT (فاصله بین شروع کمپلکس QRS تا قله R) به بیش از ۰٫۴۵ ثانیه می رسد.
- ایجاد تغییرات متقابل Reciprocal changes : عبارت از معکوس شدن انعکاسی قطعه ST در لیدهای روبروی سطح آسیب دیده به دلیل بروز ایسکمی ساب اندوکاردیال است. در انفارکتوس قدامی ، کناری و دیواره ای ، این تغییرات در لیدهای II ، III و aVF دیده می شود ، اما در انفارکتوس تحتانی ، تغییرات مذکور در لیدهای I و aVL رخ می دهد.
لازم به ذکر است که آنژین پرنیزمنتال نیز در مرحله درد می تواند تغییرات فوق را ایجاد کند ، اما این تظاهرات معمولا بعد از ۲۰ دقیقه برطرف می گردد.
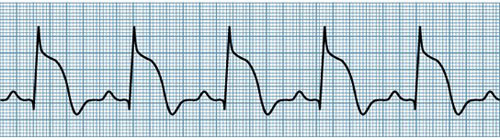
- مرحله تکمیل انفارکتوس میوکارد
- مرحله حاد انفارکتوس میوکارد
Fully Evolved MI : مرحله بینابینی انفارکتوس فوق حاد و حاد بوده ، طی آن موج T بی فازیک شده ، و به تدریج قطعه ST پایین می آید.
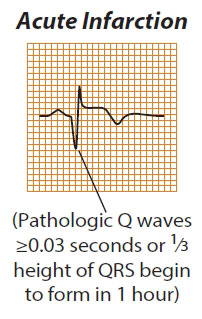 Acute MI : معمولا ۶ ساعت پس از بروز درد قلبی ، انفارکتوس تکمیل می شود و بیمار وارد مرحله حاد می گردد . در این مرحله ، تداوم درد به منزله ادامه گسترش ایسکمی است ، زیرا همانطور که گفته شد ، بافت نکروز فاقد درد است.
Acute MI : معمولا ۶ ساعت پس از بروز درد قلبی ، انفارکتوس تکمیل می شود و بیمار وارد مرحله حاد می گردد . در این مرحله ، تداوم درد به منزله ادامه گسترش ایسکمی است ، زیرا همانطور که گفته شد ، بافت نکروز فاقد درد است.
تنها معیار بروز نکروز، حضور موج Q غیر طبیعی است. هر چقدر عمق موج Q بیشتر و یا زمان آن بیشتر باشد ، وسعت نکروز نیز زیادتر است.
- بالا رفتگی خط ST از خط ایزومتریک در نواحی آزرده
- موج T معکوس یا invert در نواحی آزرده
- کاهش یا از بین رفتن بخش مثبت کمپلکس QRS در نواحی آزرده
- بروز موج Q پاتولوژیک در نواحی آزرده
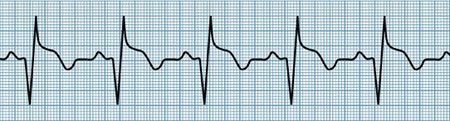
- مرحله مزمن انفارکتوس میوکارد
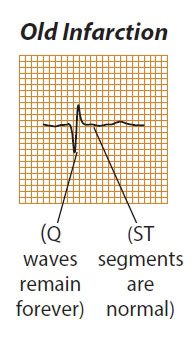 Old MI : معمولا بعد از ۳ الی ۴ هفته از بروز انفارکتوس ، ناحیه انفارکته شروع به فیبروزه شدن می کند . در این مرحله قطعه ST مجددا به حالت اولیه خود روی خط ایزومتریک برمی گردد . موج T معکوس نیز به سمت صاف شدن تمایل پیدا می کند و سال ها به همین شکل باقی می ماند . در ۲ تا ۱۰% بیماران ، T ممکن است مثبت شود.
Old MI : معمولا بعد از ۳ الی ۴ هفته از بروز انفارکتوس ، ناحیه انفارکته شروع به فیبروزه شدن می کند . در این مرحله قطعه ST مجددا به حالت اولیه خود روی خط ایزومتریک برمی گردد . موج T معکوس نیز به سمت صاف شدن تمایل پیدا می کند و سال ها به همین شکل باقی می ماند . در ۲ تا ۱۰% بیماران ، T ممکن است مثبت شود.
حتی کمپلکس GRS نیز به مرور زمان تغییر شکل داده ، به حالت طبیعی برمی گردد . به همین دلیل معمولا بعد از گذشت سه سال از انفارکتوس میوکارد ، تشخیص آن از روی نوار الکتروکاردیوگرام مشکل می شود و ممکن است نیاز به انجام تست تالیوم جهت مشخص کردن نواحی انفارکته وجود داشته باشد.
بطور کلی ، ناحیه انفارکته بافت مرده ای را تشکیل می دهد که در فعالیت های الکتریکی قلب شرکت نمی کند . به عبارت دیگر ، ناحیه مرده حکم یک پنجره را بازی می کند . به این ترتیب الکترودی که روبروی این پنجره قرار می گیرد ، فعالیت های الکتریکی نواحی سالم را منعکس می کند . به دلیل آنکه بردار این فعالیت های الکتریکی از الکترود روبروی ناحیه مرده دور می شود ، در اشتقاق مربوطه موج پایین رونده ای ثبت می شود که شکل کمپلکس QRS را کاملا تغییر می دهد و آن را یا به صورت کمپلکس QS و یا به صورت کمپلکس Qr در می آورد.
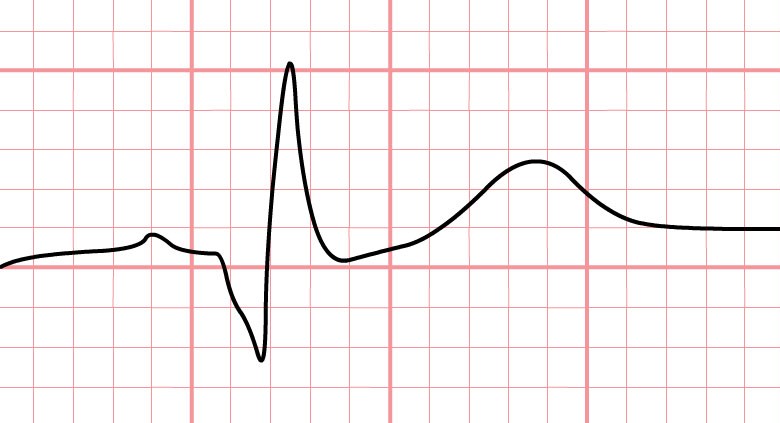
این موج پایین رونده ، اصطلاحا Q پاتولوژیک خوانده می شود. Q پاتولوژیک باید دارای شرایط زیر باشد:
- پهنای آن باید از ۰٫۰۴ ثانیه بیشتر باشد.
- در صورتی که به صورت کمپلکس QS ظاهر شود لااقل ۳ میلی متر عمق داشته باشد.
- در صورتی که به صورت کمپلکس Qr ظاهر شود ، ارتفاع آن باید لااقل ۱/۳ (یک سوم) ارتفاع R باشد.
وجود کمپلکس QS نشان دهنده انفارکتوس ترانس مورال است که در آن الکترود روبروی پنجره ، فقط فعالیت های سمت مقابل را ثبت می کند. کمپلکس Qr معمولا زمانی ایجاد می شود که لایه ای از بافت زیر اندوکارد یا زیر اپیکارد ، نکروز نشده باشد . در واقع موج کوچک r نمایانگر دپولاریزاسیون بافت باقیمانده میوکارد است.
تقسیم بندی انفارکتوس میوکارد براساس ناحیه انفارکته
انفارکتوس میوکارد براساس ناحیه انفارکته در عضله به چهار نوع تقسیم می کنند.
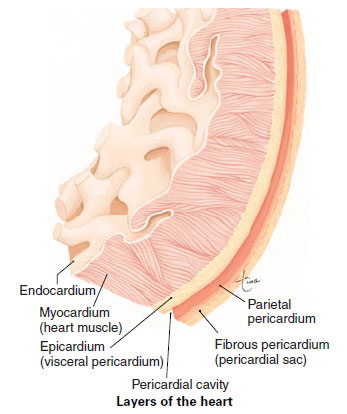
- انفارکتوس ترانس مورال : شامل نکروز کلیه لایه های قلب یعنی اندوکارد ، میوکارد و اپیکارد است . تغییرات الکتروکاردیوگرافیکی به صورت ایجاد موج Q پاتولوژیک و برجسته شدن قطعه ST است . علایم بالینی آن می تواند شامل علایم نارسایی قلبی ، ترومبوس مورال و پریکاردیت باشد.
- انفارکتوس ساب اندوکاردیال : شامل نکروز اندوکارد و میوکارد است. تغییرات الکتروکاردیوگرافیک آن به صورت سقوط قطعه ST بدون وجود Q پاتولوژیک است. علایم بالینی آن می تواند شامل نارسایی قلبی و ترومبوس مورال باشد.
- انفارکتوس ساب اپیکاردیال : شامل نکروز اپیکارد و میوکارد است. تغییرات الکتروکاردیوگرافیک آن به صورت بالارفتگی قطعه ST بدون وجود Q پاتولوژیک است. علایم بالینی آن می تواند شامل نارسایی قلبی و پریکاردیت باشد.
- انفارکتوس اینترامورال : شامل نکروز میوکارد است . تغییرات الکتروکاردیوگرافیک آن می تواند به صورت معکوس شدن موج T و کاهش ولتاژ R باشد. از نظر بالینی ، بیمار علایم نارسایی قلب را از خود نشان می دهد.
Non Qwave MI
بطور کلی انفارکتوس میوکارد را به دو دسته کلی تقسیم می کنند: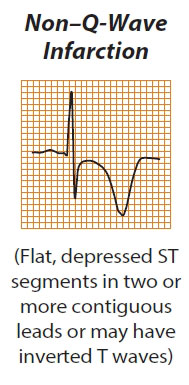
- Q Wave MI
- Non Q Wave MI
- موج Q در انفارکتوس ترانس مورال ایجاد می شود . انفارکتوس فاقد موج Q معمولا به انفارکتوس ساب اندوکاردیال اطلاق می گردد. بنابراین علایم رایج آن شامل سقوط قطعه ST همراه با افزایش آنزیم های قلبی است.
- بیش از ۵۰% بیماران بعد از ۶ ماه دچار Q Wave MI می شوند، به عبات دیگر، نکروز به سمت پریکارد پیشرفت می کند . به همین دلیل آنژیوگرافی از این افراد ضرورت دارد .
- در این نوع انفارکتوس احتمال بروز آریتمی بسیار بالا است . آریتمی مربوط به میوکارد سالم بوده ، منشا آن ، محل اتصال میوکارد سالم به بافت نکروز است . این آریتمی ممکن است حتی یک روز بعد از MI نیز ظاهر شود.
بازسازی بافت نکروزه میوکارد
Remodeling معمولا ۲۴ ساعت پس از ایجاد نکروز ، گلبول های سفید به منطقه هجوم می آورند تا نسج نکروزه را از بین ببرند. این مسئله باعث پهن شدن ناحیه می گردد (Expansion). به دنبال آن ، نسج مجددا نازک شده (Thining)، و سپس اتساع رخ می دهد (Dilatation). این ناحیه متسع شده ، بی حرکت است و در فعالیت های قلبی شرکت نمی کند.
سه مرحله فوق را بازسازی می نامند که در ۱۰% بیماران به صورت کامل دیده می شود . به دنبال بازسازی میوکارد ، گاهی بافت سالم اطراف ، شروع به تحرک بیشتر می نمایند (hyperkinesy) و باعث می شوند ناحیه بازسازی شده ، به طرف بیرون رانده شود و در نهایت تبدیل به آنوریسم گردد.
- اگر بعد از دو هفته از وقوع MI ، قطعه ST ایزومتریک نشد و همچنان به صورت بالارفتگی باقی ماند ، احتمال بروز آنوریسم وجود دارد . و اگر بعد از سه ماه ، قطعه ST همچنان دچار بالا رفتگی بود، تشخیص آنوریسم قطعی است.
- آنوریسم در هنگام سیستول بطنی ، دارای حرکت پارادوکس است . چون محل اتصال بافت سالم به آنوریسم دائما در حال کشیدگی است ، احتمال بروز درد قفسه سینه وجود دارد.
- اگر بتوان توسط اقدامات دارویی ، جلوی بازسازی میوکارد و تبدیل دیلاتاسیون به آنوریسم را گرفت ، می توان از بسیاری از عوارض مربوط به آن پیشگیری نمود.
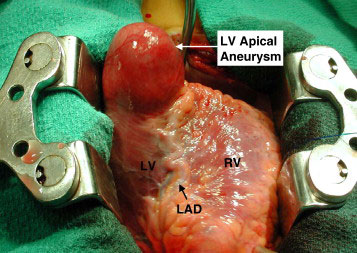
- کاهش برون ده قلبی : می تواند موجب ناراسایی قلبی گردد . هرچه آنوریسم بزرگ تر باشد ، میزان تجمع خون در آن بیشتر بوده ، نارسایی قلبی شدیدتر خواهد شد.
- درد قفسه سینه : بعد از چند روز تا چند هفته از ایجاد آنوریسم ایجاد می شود . این درد به درمان دارویی پاسخ نداده ، تغییرات ECG ایسکمی را نیز ایجاد نمی کند.
- آریتمی مقاوم به درمان : این آریتمی ها در حلقه ی دور بافت نکروزه ایجاد شده ، قابلیت بروز پدیده ورود مجدد یا Re-entry را دارد.
- ترومبوآمبولی : به دنبال تجمع خون در آنوریسم ، ترومبوس مورال ایجاد می شود که در صورت کنده شدن می تواند منجر به آمبولی سیستمیک گردد.
اثر وسعت نکروز میوکارد روی علایم بالینی
بعد از آنکه نکروز به حداکثر میزان خود رسید ، بررسی اثرات آن بر روی علایم بالینی دارای اهمیت است.
- نکروز ۱۰% : منجر به سفتی یا Stiffness میوکارد شده ، باعث می گردد میوکارد در زمان دیاستول به خوبی باز نشود . به این ترتیب کمپلیانس بطن کاهش یافته ، صدای S4 در سمع قلب شنیده می شود .
- نکروز ۱۵% : باعث بدکاری دیاستول بطن چپ می گردد ، بدین مفهوم که در زمان دیاستول ، بطن به خوبی باز نشده ، خون نمی تواند به راحتی وارد آن گردد . در چنین وضعیتی بیمار دچار تنگی نفس ، PND، ارتوپنه و ادم ریه می شود .
- نکروز ۲۰% : علایم واضح CHF و بدکاری سیستولیک ظاهر می شود . صدای S3 و رال مرطوب شنیده می شود.
- نکروز ۲۵% : بیمار در استراحت هم دچار تنگی نفس است . بیش از نیمی از ریه دارای رال مرطوب است.
- نکروز ۳۰% : علایم ادم حاد ریه ظاهر می شود.
- نکروز ۴۰% : بیمار وارد شوک کاردیوژنیک می شود.
تعیین مناطق انفارکتوس میوکارد در بطن چپ
وجود تغییرات توضیح داده شده در الکتروکاردیوگرام ، در لیدهای خاص می تواند نمایانگر منطقه انفارکتوس در بطن چپ باشد.
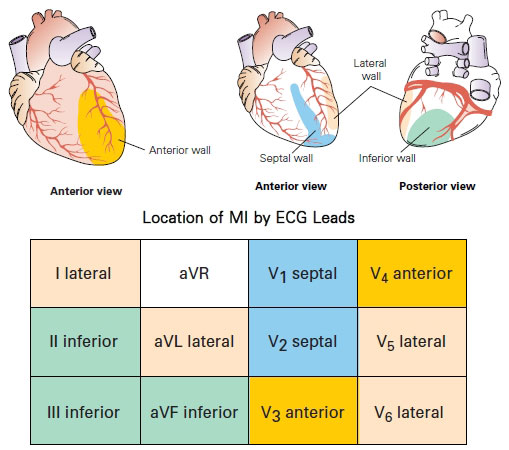
- Inferior MI
- high-lateral MI
- anterio – septal MI
- Mid – lateral MI
- lateral MI
- anterior MI
- Extensive anterior – lateral MI
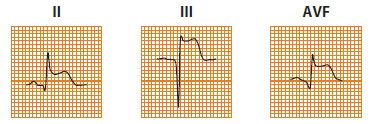
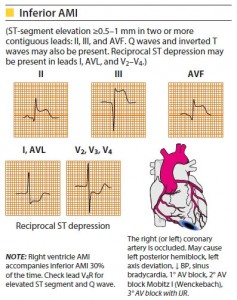
انفارکتوس دیواره تحتانی بطن چپ :
- به دنبال انسداد در شریان کرونر راست ایجاد می شود.
- تغییرات در لیدهای II و III و aVF ظاهر می گردد.
- مشاهده تغییرات الکتروکاردیوگرافیک در دو لید از سه لید فوق کافی است.
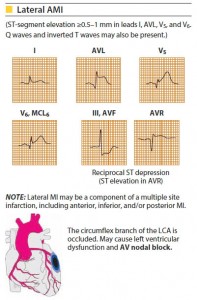
انفارکتوس دیواره کناری – فوقانی بطن چپ :
- به دلیل انسداد در شریان سیر کومفلکس چپ (LCX) ایجاد می شود.
- تغییرات در لیدهای I و aVF قابل ملاحظه است.
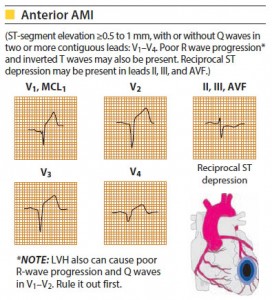
انفارکتوس دیواره ای – قدامی بطن چپ :
- به دنبال انسداد در شریان نزولی قدامی چپ (LAD) ایجاد می گردد .
- تغییرات در لیدهای V1 تا V4 مشاهده می شود.
انفارکتوس کناری – تحتانی بطن چپ :
- به دلیل انسداد در شریان نزولی قدامی چپ (LAD) ایجاد می شود.
- تغییرات در لیدهای V5 و V6 مشهود است.
انفارکتوس دیواره کناری بطن چپ :
- به دنبال انسداد در شریان سیر کومفلکس چپ (LCX) و نزولی قدامی چپ (LAD) ایجاد می گردد.
- تغییرات در لیدهای I، aVF، V5 و V6 قابل بررسی است.
انفارکتوس دیواره قدامی بطن چپ :
- به دلیل انسداد شریان نزولی قدامی چپ (LAD) ایجاد می شود.
- تغییرات در لیدهای V1 تا V6 مشاهده می گردد.
انفارکتوس وسیع قدامی – کناری بطن چپ :
- به دنبال انسداد شریان سیر کومفلکس چپ ایجاد می شود .
- تغییرات به صورت تصویر آینه ای (Changes mirror) در لیدهای V1 و V2 مشهود است.
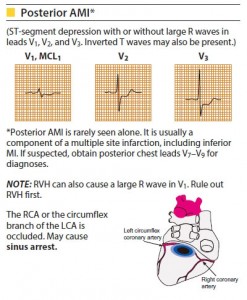
- بدلیل آنکه هیچ یک از ۱۲ لید استاندارد قادر به ثبت مستقیم فعالیت های ناحیه خلفی بطن چپ نیستند ، لذا برای توضیح وجود انفارکتوس ناحیه خلفی ، باید تغییرات معکوس یا تصویر آینه ای آن را روی الکترودهای مقابل سطح آسیب دیده (یعنی V1 و V2 ) مورد بررسی قرار داد .
- انفارکتوس دیواره خلفی معمولا به ندرت به تنهایی ایجاد می شود و اغلب همیشه با انفارکتوس دیواره تحتانی بطن چپ همراه است.
تغییرات الکتروکاردیوگرافیک آینه ای در لیدهای V1 و V2 عبارتند از:
- وجود موج R بلند با پهنایی بیشتر از ۰۴/۰ ثانیه
- نسبت R به S بیشتر از ۱، یعنی R بلندتر از S است
- پایین رفتگی قطعه ST
- بالارفتگی قطعه ST به میزان یک میلیمتر یا بیشتر در لیدهای V7، V8، V9.
(این لیدها در پنجمین فضای بین دنده ای، به ترتیب روی خطوط پوستریور آگزیلاری، میداسکاپولار ، و مید ورتبرال قرار می گیرند).
اقدامات درمانی اورژانسی در انفارکتوس حاد میوکارد
در صورت پذیرش بیمار با تشحیص انفارکتوس حاد میوکارد ، باید اقدامات درمانی زیر براساس پروتکل توسط پرستاران بخش CCU به مورد اجرا درآید.
الف) تسکین درد بیمار
اولین و مهمترین اقدام درمانی در بیماران مبتلا به انفارکتوس حاد میوکارد ، تسکین درد قلبی است . زیرا می تواند باعث آزاد شدن کاتکولامین ها و وخیم تر شدن وضعیت بیمار گردد . کنترل درد از طریق چهار اقدام زیر صورت می گیرد:
- استراحت مطلق :
- تجویز اکسیژن :
- انفوزیون وریدی TNG :
- مسکن مخدر :
پس از انتقال برروی تخت ، بیمار باید در وضعیت نیمه نشسته قرار گیرد . هدف از حفظ این وضعیت ، بالاتر نگهداشتن سطح قلب از سایر اندام های بدن است . در صورتیکه فشار خون سیستولیک بیمار کمتر از ۹۰mmHg باشد ، نباید سرتخت را بیش از ۲۰ درجه بالا برد . بدین منظور می توان بالشی را زیر ناحیه کتف سر و گردن بیمار قرار داد . بدین ترتیب سطح قلب همچنان بالاتر از سطح اندام های بدن قرار می گیرد . معمولا بیماران به مدت ۴۸ ساعت در وضعیت استراحت مطلق باقی می مانند.
اکسیژن جهت بهبودی درد ، سیانوز و تنگی نفس بیمار تجویز می گردد . میزان تجویز اکسیژن ۲ تا ۴ لیتر در دقیقه است . به دلیل آنکه اغلب بیماران مبتلا به انفارکتوس میوکارد دچار بیماری های مزمن انسدادی ریه (COPD) هستند ، تجویز مقادیر بالاتر اکسیژن توصیه نمی شود . اکسیژن باید توسط کانولای بینی داده شود ، زیرا مقادیر زیر ۶ لیتر در دقیقه ، نمی تواند درصد مناسب اکسیژن را توسط ماسک ساده صورت تامین نماید.
- وازودیلاتورهای وابسته به EDRF
- وازودیلاتورهای غیر وابسته به EDRF
- EDRF یا Endothelial Drive Relaxation Factor ، ماده ای است که از اندوتلیوم رگ های سالم آزاد شده ، باعث شل شن عضله رگ می شود . در صورت پاره شدن ، تخریب یا آترواسکلروزه شدن رگ ، این ماده ترشح نمی شود . TNG جزو وازودیلاتورهای غیر وابسته به EDRF است ، بنابراین هم عروق آترواسکلروتیک و هم سالم را گشاد می کند .
- TNG توسط اتساع شریان های کولترال قلب ، و جلوگیری از اسپاسم عروق کرونر ، خونرسانی به قلب را تسهیل کرده ، موجب تخفیف درد قلبی می گردد .
- انفوزیون TNG را با ۵-۱۰ ?g/min آغاز کرده ، همزمان با آن شدت درد و میزان فشار خون بیمار را کنترل می کنند . در صورت تداوم درد ، هر ۵ دقیقه ۵ ?g/min به دوز قبلی اضافه می کنند تا وضع بیمار تثبیت گردد . حداکثر دوزی که می توان برای بیمار تجویز نمود، ۲۰۰ ?g/min است.
- پس از تثبیت وضعیت بیمار از نظر تسکین درد قلبی و فشار خون ، به منظور قطع کردن این دارو باید به ترتیب هر ۱۰ دقیقه ۵ ?g از دوز دارو کاست تا نهایتا به میزان اولیه ۵-۱۰ ?g/min رسید.(Tapering). سپس می توان انفوزیون را کاملا قطع کرد.
 داروی انتخابی جهت تسکین درد قلبی ، سولفات مورفین است که یک ونودیلاتور بسیار قوی بوده ، باعث کاهش پیش بار و افت فشار ویج مویرگ های ریوی می شود . لذا این ضمن تسکین درد ، موجب از بین رفتن اضطراب و کاهش فشار خون نیز می شود. در صورتی که فشار خون سیستولیک بیمار بالاتر از ۹۰mmHg و نبض وی بیشتر از ۵۰ ضربه در دقیقه باشد، می توان سولفات مورفین را به میزان ۳ تا ۵ میلی گرم آهسته وریدی و به صورت رقیق شده به بیمار تزریق نمود . در صورت تداوم درد می توان دارو را هر ۵ دقیقه تا دوز نهایی ۲-۳ mg/Kg تجویز نمود . توجه به میوز مردمک ها جهت تشخیص رسیدن به دوز درمانی مناسب می تواند کمک کننده باشد.
داروی انتخابی جهت تسکین درد قلبی ، سولفات مورفین است که یک ونودیلاتور بسیار قوی بوده ، باعث کاهش پیش بار و افت فشار ویج مویرگ های ریوی می شود . لذا این ضمن تسکین درد ، موجب از بین رفتن اضطراب و کاهش فشار خون نیز می شود. در صورتی که فشار خون سیستولیک بیمار بالاتر از ۹۰mmHg و نبض وی بیشتر از ۵۰ ضربه در دقیقه باشد، می توان سولفات مورفین را به میزان ۳ تا ۵ میلی گرم آهسته وریدی و به صورت رقیق شده به بیمار تزریق نمود . در صورت تداوم درد می توان دارو را هر ۵ دقیقه تا دوز نهایی ۲-۳ mg/Kg تجویز نمود . توجه به میوز مردمک ها جهت تشخیص رسیدن به دوز درمانی مناسب می تواند کمک کننده باشد.
از عوارض عمده TNG، افت فشار خون است که باید مرتبا هر ۱۵ دقیقه مورد کنترل قرار گیرد.
در صورت بروز هر یک از علایم زیر باید انفوزیون دارو را قطع نمود :
- توقف درد قلبی
- افزایش ریت قلب از ۱۰۰ ضربه در دقیقه
- کاهش فشار خون سیستولیک به زیر ۹۰mmHg
عوارض مهم مربوط به تجویز سولفات مورفین که باید به دقت تحت کنترل قرار گیرد عبارتند از:
- دپرسیون مرکز تنفس
- برادی کاردی
- افت فشارخون
- تهوع و استفراغ
- خواب آلودگی و کانفیوژن
در صورتیکه فشار خون سیستولیک بیمار کمتر از ۹۰mmHg باشد ، بهتر است از مورفین استفاده نشود . پتدین (پنتازوسین) ، به دلیل اثرات آنتی کولینرژیکی که دارند ، باعث بروز تاکیکاردی می شوند . لذا مصرف آنها به عنوان ضد درد در MI می تواند خطرساز باشد. به علاوه این داروها بر میزان تهوع و استفراغ بیمار می افزایند . داروی مخدر متادون نیز به دلیل عوارض هیپوتانسیون و تهوع ، در MI مورد مصرف ندارد.
- ظاهرا این طور به نظر می رسد که اگر نتوان به بیمار با درد قلبی مورفین تجویز کرد ، بهتر است از مخدر دیگری استفاده نشود.
ب) جلوگیری از بروز آریتمی
- مانیتورینگ دائم قلب :
- کنترل علایم حیاتی :
- تجویز لیدوکایین :
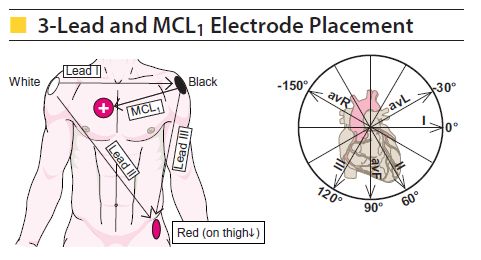
توسط مانیتورینگ یکی از لیدهای MCL1، MCL6 و M3 می توان اطلاعات مفیدی در مورد عملکرد قلب به دست آورد.
- جهت ثبت لید MCL1 ، الکترود دست چپ روی ناحیه V1 ، الکترود دست راست روی کتف چپ ، و الکترود پای راست روی کتف راست قرار می گیرد.
- به منظور ثبت لید MCL6 ، الکترود دست چپ روی ناحیه V6 ، الکترود دست راست روی کتف چپ ، و الکترود پای راست روی کتف راست قرار می گیرد.
- جهت ثبت لید M3، الکترود دست چپ در ناحیه فوقانی چپ شکم ، الکترود دست راست روی کتف چپ ، و الکترود پای راست روی کتف راست قرار می گیرد.
این علایم حیاتی شامل موارد زیر هستند:
- کنترل نبض از نظر تعداد ، نظم و کیفیت
- مقایسه نبض اپیکال و رادیال
- بررسی فشار نبض (اختلاف بین فشار خون سیستول و دیاستول)
- بررسی فشار متوسط شریانی براساس فرمول زیر:
MAP: 1/3S + 2/3D
- بررسی تنفس از نظر تعداد و عمق و نظم
- بررسی سطح هوشیاری بیمار
- بررسی علایم حیاتی پوست ، شامل رنگ ، حرارت و رطوبت انتهاها
این دارو در اکثر آریتمی های re-entrant بطنی موثر است و بخصوص جهت کنترل انقباضات زودرس بطنی (PVC) ، در صورتی که باعث تغییرات همودینامیک شده باشند مورد استفاده قرار می گیرد.

در صورت بروز PVC های منظم نظیر بای ژمینی و نیز تاکی آریتمی های بطنی ، می توان از دور بلوس این دارو به میزان ۱mg/Kg استفاده کرد. با تزریق دوز حمله ای، لیدوکایین به سطح درمانی خود در خون می رسد و موثر واقع می شود. اثر دوز بلوس بعد از ۳۰ دقیقه به حداکثر خود رسیده ، و پس از ۶۰ دقیقه مجددا به زیر خط درمانی نزول پیدا می کند و در همین جاست که بیمار مجددا دچار آریتمی می شود . به همین دلیل همیشه باید ۳۰ دقیقه پس از تجویز دوز بلوس لیدوکایین ، نصف این دوز را (۰٫۵mg/Kg) مجددا به بیمار تزریق کرد . بدین ترتیب دوز نگهدارنده دارو (انفوزیون مداوم ۱-۴mg/min) می تواند سطح درمانی دارو را در بدن حفظ نماید.

درمورد کنترل ضربانات نبض باید توجه داشت که هر یک از ضربانات قلب که به دنبال خود نبض ایجاد نمی کند ، در واقع فاقد حجم ضربه ای موثر بوده ، در نهایت باعث کاهش برون ده قلبی می گردد . هرچه تعداد این ناهماهنگی بین ضربانات قلب و نبض بیشتر باشد ، نمایانگر از دست دادن تعداد زیادتری از حجم های ضربه ای بوده و در نهایت می تواند منجر به بروز علایم تغییرات همودینامیک در بیمار شود . در چنین مواردی ملاحظات دارویی ، مثل تجویز لیدوکایین برای کنترل PVC ضرورت می یابد . در غیر این صورت فقط باید بیمار را از نظر بروز علایم تغییرات همودینامیک تحت نظر قرار داد.
توجه به فشار متوسط شریانی نیز از اهمیت ویژه ای برخوردار است . در بیمارانی که در آنها میزان MAP به کمتر از ۷۰mmHg افت کرده باشد ، باید دقیقا علایم شوک کاردیوژنیک را تحت نظر قرار داد . کاهش MAP همراه با پوست سرد و مرطوب و کاهش سطح هوشیاری ، یک علامت خطر مهم تلقی می گردد.
ج) سایر اقدامات درمانی:
- تهیه نمونه خون : این نمونه خون جهت انجام آزمایشات بیوشیمی (قند ، BUN ، کراتینین ، سدیم ، پتاسیم ، آنزیم های قلبی) ، هماتولوژی و آزمایشات انعقادی خون تهیه و فرستاده می شود . همچنین نمونه جهت آزمایش کامل ادرار نیز تهیه می شود . آنزیم های قلبی را باید در بدو ورود ، ۱۲ ساعت ، ۲۴ ساعت ، و ۴۸ ساعت بعد کنترل نمود.
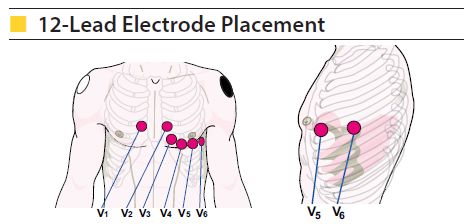
- ثبت نوار الکتروکاردیوگرام از ۱۲ لید : به منظور بررسی تغییرات مربوط به پیشرفت ایسکمی میوکارد ، باید در بدو ورود، ۱۲ ساعت و ۲۴ ساعت بعد و سپس روزانه از بیمار ECG از ۱۲ لید کنترل شود.
- تجویز هپارین : هپارین با تحریک آنتی ترومبین III از تبدیل پروترومبین به ترومبین و فیبرینوژن جلوگیری می کند. تجویز هپارین یک اقدام مهم جهت پیشگیری از پیشرفت ترومبوز در داخل عروق نواحی گرفتار و نیز ترومبوس مورال است.
اولین دوز هپارین، ۵۰۰۰ واحد داخل وریدی بوده، دوزهای بعدی یا به صورت انفوزیون مداوم ۱۰۰۰u/h و یا به صورت وریدی (تا ۵۰۰۰ هر ۶ ساعت) یا زیرجلدی (۵۰۰۰u هر ۱۲ ساعت) همراه با کنترل PTT تجویز می گردد.
اقدامات درمانی اورژانس در انفارکتوس فوق حاد میوکارد
پس از قطعی شدن تشخیص انفارکتوس فوق حاد میوکارد، اساس اقدامات درمانی بر محدود کردن نکروز یا Infarct Limitation گذاشته می شود. این کار از طریق استفاده از چهار داروی زیر انجام می گیرد:
- الف) استرپتوکیناز
- ب) TNGوریدی
- ج) بتابلوکرها
- د) سولفات منیزیوم
کلیه عوامل فوق باعث برقراری جریان خون کرونر ، و کاهش تقاضای اکسیژن میوکارد می شوند.
الف) استرپتوکیناز :
 SK استرپتوکیناز یک داروی فیبرینولیتیک است که از استرپتوکوک بتا همولیتیک به دست می آید . این دارو موجب تبدیل پلاسمینوژن به پلاسمین می گردد که خود عامل حل کردن فیبرین است . با حل شدن فیبرین در انشعابات مسدود شده عروق کرونر ، گردش خون مجددا برقرار می گردد و به این ترتیب از بروز نکروز یا پیشرفت آن جلوگیری می شود.
SK استرپتوکیناز یک داروی فیبرینولیتیک است که از استرپتوکوک بتا همولیتیک به دست می آید . این دارو موجب تبدیل پلاسمینوژن به پلاسمین می گردد که خود عامل حل کردن فیبرین است . با حل شدن فیبرین در انشعابات مسدود شده عروق کرونر ، گردش خون مجددا برقرار می گردد و به این ترتیب از بروز نکروز یا پیشرفت آن جلوگیری می شود.
این دارو دارای اثر سریع بوده ، بهترین زمان تزریق آن ۴ تا ۶ ساعت بعد از وقوع MI است . پس از کنترل دو ECG و مشاهده علایم زیر ، می توان تشخیص MI فوق حاد را تایید و استرپتوکیناز را آغاز نمود :
- بالارفتگی قطعه ST در لیدهای مجاور : این بالا رفتگی باید در لیدهای اعضا حداقل یک میلیمتر و در لیدهای جلوی قلبی حداقل ۲ میلیمتر باشد.
- توجه به انحنای قطعه ST : انحنای قطعه DT باید رو به بالا باشد .
- وجود موج T مثبت و نوک تیز (upright)
انتخاب بیمار برای تجویز استرپتوکیناز
استرپتوکیناز داروی پر عارضه ای محسوب می شود . این دارو دارای دو عارضه بالقوه ، یعنی خونریزی و واکنش های آلرژیک، و یک عارضه ثانویه به پرفیوژن مجدد عروق کرونر ، یعنی آریتمی های خطرناک است ، بنابراین باید بیمار کاندید تزریق استرپتوکیناز را به دقت انتخاب نمود تا مشکلات ناشی از عوارض را به حداقل رساند.
- سن بیمار زیر ۷۵ باشد .
- بیمار سابقه اختلالات گوارشی از قبیل زخم یا التهاب را نداشته باشد .
- در شش ماه گذشته هیچگونه عمل جراحی نداشته باشد .
- سابقه CVA ، تومور مغزی و ضربه مغزی نداشته باشد .
- سابقه هیچگونه پیوند اعضا را نداشته باشد .
- حامله نباشد .
- فشار خون بیمار بالاتر از ۱۱۰/۲۰۰ نباشد .
- احیای قلبی ریوی طولانی یا تروماتیک نداشته باشد .
- تحت درمان با داروهای آنتی کوآگولانت نباشد .
- طی یک سال گذشته ، توسط استرپتوکیناز تحت درمان قرار نگرفته باشد .
توجه ۱ :
- تجویز استرپتوکیناز در مبتلایان به انفارکتوس تحتانی باید با احتیاط و دقت صورت گیرد.
- در صورتی که بیمار به تنهایی دچار انفارکتوس تحتانی شده باشد ، معمولا از تجویز دارو خودداری می شود ، زیرا امکان ایجاد انفارکتوس قدامی که خطرناک تر است ، طی یک سال آینده وجود دارد . بنابراین شانس دریافت استرپتوکیناز را برای انفارکتوس قدامی باز می گذارند.
- در صورتی که بیمار در گذشته دچار انفارکتوس قدامی شده ، و اکنون نیز مبتلا به انفارکتوس تحتانی باشد ، از استرپتوکیناز استفاده می شود.
- در صورت همراه بودن انفارکتوس تحتانی با انفارکتوس خلفی ، یا انفاکتوس بطن راست از استرپتوکیناز استفاده می شود.
توجه ۲ :
یکی از عوارض تزریق استرپتوکیناز ، ایجاد واکنش ایمیون کمپلکس است که طی آن ، استرپتوکیناز به صورت آنتی ژن عمل می کند و بدن در مقابل آن آنتی بادی می سازد . این واکنش ایمیون کمپلکس تا یکسال در بدن باقی می ماند . بنابراین تزریق مجدد این دارو طی این یکسال می تواند باعث بروز واکنش های آلرژیک و حتی آنافیلاکسی گردد.
نکات مهم در تجویز استرپتوکیناز
جهت درمان با این دارو ، به ۱٫۵ میلیون واحد استرپتوکیناز (دو ویال ۷۵۰ هزار واحدی) نیاز است که در مدت زمان یک ساعت انفوزیون می شود . البته در افراد سالمند توصیه شده است که مدت زمان انفوزیون را طولانی تر کرده ، حتی به دو ساعت برسانند.
پروتئینهای استرپتوکیناز بسیار شکننده هستند ، لذا جهت حل کردن آنها باید حلال را با یک سر سوزن قطور و به آرامی وارد ویال کرد ، به طوری که دارو کف نکند . جهت حل کردن دارو نباید ویال را به شدت تکان داد ، بلکه باید آن را بین دو دست غلطاند . پس از حل شدن دارو ، باید آن را به آرامی و توسط یک سرسوزن قطور به درون میکروست محتوی ۵۰ تا ۱۰۰ میلی لیتر دکستروز ۵% وارد کرد . بین تجویز دو ویال استرپتوکیناز نباید فاصله زمانی بیفتد.
نکات زیر را باید پیش از شروع انفوزیون دارو رعایت نمود:
- قبل از تجویز دارو ، بیمار باید حتما دو رگ مناسب و باز داشته باشد .
- گروه خون ، کراس ماچ و TT (ترومبین تایم) باید کنترل شود .
- باید دو ECG به فاصله نیم ساعت از بیمار وجود داشته باشد که در آن علایم انفارکتوس فوق حاد مورد تایید قرار گرفته باشد.
- حتما باید پیش از شروع کار ، انفوزیون TNG برای بیمار آغاز شود . همزمان با تجویز TNG، باید به فشارخون ، درد قفسه سینه ، و ریت قلبی بیمار توجه شود . در صورت افزایش ریت قلب به بالای ۱۱۰ ضربه در دقیقه، باید دوز دارو را کم نمود.
- تجویز پروفیلاکسی لیدوکایین ضرورتی ندارد ، اما باید آماده و بالای سر بیمار باشد تا به محض شروع آریتمی ، ابتدا با دوز بلوس ۱٫۵ – ۱ mg/Kg آغاز و سپس با دوز نگهدارنده ۱mg/Kg دنبال شود . معمولا انفوزیون لیدوکایین تا ۶ ساعت بعد از تجویز استرپتوکیناز ادامه می یابد.
- تجویز استروئیدها و هیدروکورتیزون به منظور پیشگیری از واکنش های آلرژیک توصیه نمی شود زیرا موارد گزارش شده از حساسیت کم بوده ، و بین ۰٫۲ – ۰٫۱ % است . به علاوه چون استروئیدها روند ترمیم زخم را به تاخیر می اندازند ، خطرناک هستند.
- در صورت بروز واکنش های آلرژیک ، ترجیح داده می شود از داروهای آنتی هیستامین نظیر فنرگان و کلماستین وریدی استفاده شود . در غیر این صورت می توان از هیدروکورتیزون به میزان ۲۰۰mg وریدی استفاده نمود.
- در صورت بروز خونریزی ، باید از داروی آمینوکاپروئیک اسید (کاپرامول) که آنتی دوت قطعی استرپتوکیناز است استفاده کرد . تزریق این دارو ابتدا از ۱۰mg وریدی آغاز می شود و در صورت تداوم خونریزی تا ۵۰mg ادامه می یابد . در صورت عدم دسترسی به کاپرامول ، باید اقدام به ترانسفوزیون FFP نمود.
معیارهای ارزیابی تاثیر استرپتوکیناز
- توقف یا کاهش درد قفیه سینه (chest pain) . علامت افزایش عرضه خون به نواحی ایسکمیک است.
- تغییرات قطعه ST در الکتروکاردیوگرام . هنگام تصمیم درمورد انفوزیون استرپتوکیناز ، باید در سه مرحله از بیمار ECG از ۱۲ لید کنترل شود :
- بلافاصله قبل از شروع انفوزیون.
- بلافاصله بعد از اتمام انفوزیون.
- یک ساعت بعد از اتمام انفوزیون.
در هر سه ECG ، مقادیر بالارفتگی قطعه ST را در کلیه لیدها با هم جمع می کنیم (مثلا مقادیر بالارفتگی ST از V1 تا V6، برابر با ۲۰mm شده است) . اگر در ECG یک ساعت بعد ، این مقدار، ۵۰% کاهش پیدا کرد و نصف شد ، نمایانگر تاثیر استرپتوکیناز است .
- بروز آریتمی های وابسته به پرفیوژن مجدد کرونر . زمانی که ترومبوز تشکیل شده توسط استرپتوکیناز حل می شوند ، جریان خون به ناگهان برقرار شده باعث تحریک سریع منطقه ایسکمیک بخصوص در نواحی ساب اندوکاردیال می گردد . شایع ترین آریتمی های حاصله شامل PVC ، Slow VT، Rapid VT هستند.
Slow VT اختصاص به استرپتوکیناز داشته ، شامل یک ریتم ایدئوونتریکولار است که بین ۱۱۰-۷۰ ضربه در دقیقه می زند . معمولا احتیاجی به درمان و یا قطع انفوزیون استرپتوکیناز ندارد ، اما اگر ریت قلب به زیر ۷۰ ضربه در دقیقه و فشار خون سیستولیک به کمتر از ۹۰mmHg رسید ، باید اقدام به تزریق وریدی ۰٫۵mg آتروپین نمود . این کار موجب تحریک گره SA و برگشت ریتم سینوسی می شود.
در صورت بروز Rapid VT ، باید ابتدا اقدام به تجویز دوز حمله ای لیدوکایین نمود. در صورت اصلاح آریتمی، انفوزیون استرپتوکیناز ادامه می یابد، اما در صورت عدم پاسخ به درمان، باید انفوزیون را قطع کرده، به بیمار شوک کاردیوورژن داد.
- به حداکثر رسیدن زود هنگام CPK. استرپتوکیناز باعث می شود که آنزیم CPK سریعا وارد گردش خون شود ، لذا در صورت تاثیر این دارو ، بین ۱۲ تا ۱۸ ساعت بعد از MI مقدار CPK به حداکثر میزان خود می رسد . هرچه این افزایش سریع تر انجام گیرد ، برگشت آن به حد طبیعی نیز زودتر صورت می گیرد و این نشانه تاثیر مناسب استرپتوکیناز است.
توجه:
کاهش بالارفتگی قطعه ST بعد از تزریق استرپتوکیناز ، به تدریج و در خلال یک ساعت اتفاق می افتد . در صورتیکه این اصلاح بطور ناگهانی رخ دهد ، ممکن است آنژین پرنیزمنتال را مطرح سازد.
ب) انفوزیون TNG :
TNG همانطور که پیش تر نیز گفته شد ، TNG یک وازودیلاتور غیر وابسته به EDRF بوده ، می تواند هم عروق آترواسکلروزه و هم سالم را گشاد کند . به دلیل تمایل به افت فشار خون ، مصرف TNG در انفارکتوس تحتانی و بطن راست باید با احتیاط صورت گیرد.
به منظور محدود کردن ناحیه انفارکته ، باید این دارو را تا ۲۴ ساعت ادامه داد . اما در انفارکتوس تحتانی و بطن راست ، دارو را بلافاصله بعد از ساکت شدن درد قطع می کنند زیرا می تواند باعث کاهش پیش بار قلب گردد.
ج) بتابلوکرها :
β-blocker بتابلوکرها به دلیل کاهش مصرف اکسیژن میوکارد، باعث محدودیت ناحیه انفارکته شده ، بخصوص بقای بیماران مبتلا به Q Wave MI را افزایش می دهند.
- وجود درد قفسه سینه
- بالا بودن ضربانات قلب
- طبیعی یا بالا بودن فشار خون
- عدم وجود علایم مربوط به نارسایی بطن چپ (تنگی نفس، رال، S3)
- عدم وجود سابقه آسم و COPD
از این دسته دارو ها می توان به Metaprolol و Propranolol اشاره کرد.
متوپرولول یک بتابلوکر سریع اثر است که تاثیر آن خیلی زود از بین می رود . این دارو را با میزان ۵mg وریدی آغاز می کنند و سپس هر ۵ دقیقه، ۵mg بر دوز آن می افزایند تا به دوز نهایی ۱۵mg برسد.
پروپرانولول دارای اثری آهسته تر بوده ، عوارض بیشتری هم دارد و باید با احتیاط زیادتری مورد مصرف قرار گیرد . پیش از شروع این دارو باید فشار خون و نبض را کنترل کرد و اگر مقادیر آنها به ترتیب بالاتر از ۱۰۰mmHg و ۸۰ ضربه در دقیقه بود ، دارو تجویز می شود . مقدار تجویز آن ۰٫۱mg/5min است و هر ۵ دقیقه باید BP و P مجددا کنترل شود. حداکثر دوز دارو ۱۲ – ۶ mg می باشد . با تثبیت وضعیت بیمار ، دارو به صورت خوراکی ادامه می یابد و تا دو سال مصرف می شود.
د) سولفات منیزیوم

از سولفات منیزیوم به چهار دلیل زیر استفاده می شود :
- این دارو یک وازودیلاتور شریانی بوده ، عروق کرونر را نیز گشاد و عرضه خون به میوکارد را تسهیل می کند.
- یک داروی آنتی آریتمی بوده ، باعث کوتاه شدن فاصله QT و جلوگیری از بروز Polymorphic VT و آریتمی نقطه رقصان یا Torsades De Point می گردد .
- سولفات منیزیوم از تجمع پلاکتها و تشکیل میخ پلاکتی جلوگیری می کند.
- باعث بهبود عملکرد بطن چپ می گردد.
موارد منع مصرف این دارو شامل:
- ریت قلب کمتر از ۵۰ ضربه در دقیقه
- فشار خون زیر ۹۰mmHg
- اختلالات هدایتی
- نارسایی مزمن کلیه
بهتر است پیش از شروع این دارو ، مقدار منیزیوم سرم بیمار را کنترل نمود . دوز اولیه این دارو ۱۶mEq/5-10min بوده ، به دنبال آن دوز نگهدارنده به میزان ۱۲۸mEq در طی ۲۴ ساعت برای بیمار انفوزیون می شود.
انفارکتوس بطن راست
RV Mi بدکاری بطن راست به دنبال انفارکتوس بطن راست ، یکی از مهمترین اختلالاتی است که باید در بیمار مبتلا به انفارکتوس مورد توجه قرار گیرد. البته به دلیل کوچک بودن توده بطن راست ، کم بودن فشار بطن و نیز تغذیه کافی بطن راست از عروق خونی ، این نوع انفارکتوس به ندرت ایجاد می شود . معمولا انفارکتوس بطن راست همراه با انفارکتوس ترانس مورال اینفریور و پوستریور بطن چپ دیده می شود و ناشی از آترواسکلروز عروق کرونر راست و گاهی سیرکومفلکس چپ است. آسیب معمولا در دیواره خلفی ایجاد می شود که ممکن است به دیواره آزاد آنترولترال راست نیز برسد. انفارکتوس ناحیه قدامی بطن راست به دلیل خونرسانی غنی آن شایع نیست.
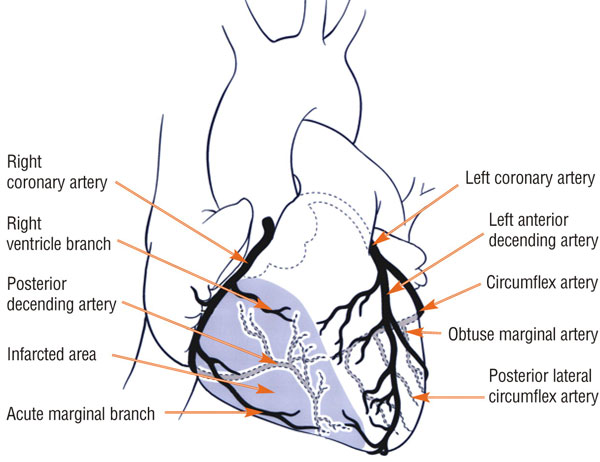
تغییرات الکتروکاردیوگرافیک ناشی از انفارکتوس بطن راست
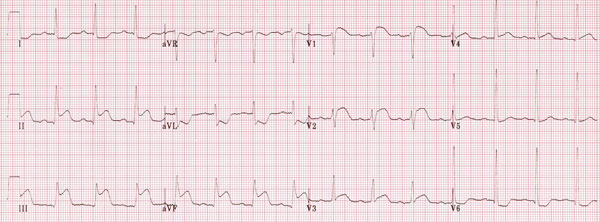
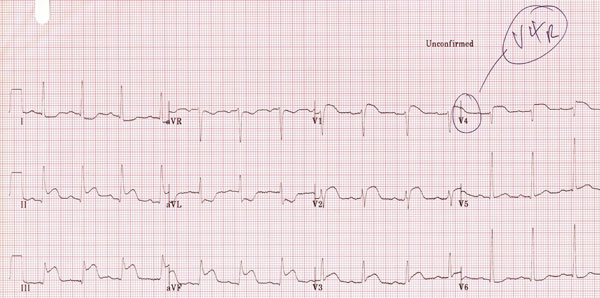
همانطور که پیشتر نیز گفته شد ، انفارکتوس تحتانی و خلفی بطن چپ اتفاق می افتد . تشخیص بر مبنای تغییرات قطعه ST است و چون این تغییرات در انفارکتوس بطن راست یک پدیده گذرا بوده معمولا بعد از گذشت ۲۴ – ۱۰ ساعت از شروع درد قلبی به حالت طبیعی بر می گردد ، باید در ابتدای پذیرش بیمار ، حتما اشتقاق های پریکاردیال سمت راست نیز کنترل شوند زیرا الکتروکاردیوگرام ۱۲ لید اصلی ، اطلاعات قطعی برای تشخیص آن به دست نمی دهد .
تغییرات الکتروگرافیک در انفارکتوس بطن راست عبارتند از :
- وجود انفارکتوس تحتانی (inferior Mi) حاد بطن چپ
- بالا رفتگی قطعه ST در لید های V1 و V2 به میزان ۰٫۵ تا ۱ میلی متر یا بیشتر
- بالا رفتگی قطعه ST در V4R تا V6R به میزان ۰٫۵ تا ۱ میلی متر یا بیشتر ، که این پدیده در V4R از همه واضح تر است .
- در صورت وجود بالا رفتگی ST در لید های جلوی قلبی ، میزان بالا رفتگی ST در V1 از همه بیشتر بوده ، هرچه به سمت جلو برویم از بالا رفتگی آن کاسته می شود .
- بالا رفتگی قطعه ST در لید III بیشتر از لید II است .
به طور کلی می توان گفت در حضور انفارکتوس تحتانی بطن چپ ، بالا رفتگی قطعه ST در لید V4R با یا بدون Q پاتولوژیک ارزش تشخیصی دارد .
اقدامات درمانی اورژانس هنگام بروز انفارکتوس بطن راست
هدف از این اقدامات از بین بردن علائم نارسایی پمپ خون توسط بطن راست است این اقدامات عبارتند از :
- تجویز سرم نرمال سالین به میزان ۲۰۰ml/h به منطور فرستادن حجم خون کافی به طرف قلب چپ و دستیابی به حداکثر پیش بار .
- مانیتورینگ فشار وج مویرگهای ریوی ( PCWP ) جهت کنترل حجم مایع انفوزیون شده و پیشگیری از صدمه به دهلیز چپ . بدین منظور باید فشار وج کاپیلرهای ریوی بین ۱۸ – ۱۵ میلی متر جیوه حفظ شود و هرگز از ۲۰ میلی متر جیوه تجاوز نکند .
- تجویز دارو های اینوتروپ مثبت نظیر دوپامین و دوبوتامین . دوپامین با دوز ۲-۵ µg/kg/min موجب دیلاتاسیون عروق کلیه و ایجاد دیورز می شود با دوز ۵-۱۰ µg/kg/min گیرنده های دوپامینرژیک را تحریک کرده ، قدرت انقباضی قلب را تقویت می کند و با دوز بالاتر از ۱۰ µg/kg/min موجب انقباض عروقی و تاکی کاردی می شود . در این میان به دلیل آنکه دوبوتامین با دوز ۲٫۵-۱۰ µg/kg/min بدون ایجاد انقباض عروقی شدید و تاکی کاردی ، همان اثر اینوتروپ را روی قلب دارد ، داروی انتخابی اول به حساب می آید .
- در صورت بروز هایپوتانسیون ، بلوک های قلبی و کاهش برون ده قلب ، می توان از پیس میکر موقت استفاده کرد .
- کنترل علائم حیاتی بیمار شامل فشار خون ، فشار متوسط شریانی ، نبض ، تنفس سطح هوشیاری
- کنترل پوست و انتهاها از نظر سردی و رطوبت ، سیانوز و ادم محیطی
- مشاهده اتساع ورید های گردنی
- سمع ناحیه LBS قلب
- مانیتورینگ V4R و ثبت استریپ آن در هر ۴ ساعت
- ارزیابی بیمار از نظر بروز علائم نارسایی ثانویه بطن چپ
- تجویز دیورتیک ها
- تجویز ونودیلاتور ها ( TNG و مورفین )
- دادن پوزیشن نشسته به بیمار
- مانور والسالوا
عوارض انفارکتوس میوکارد
عوارض انفارکتوس میوکارد به سه دسته تقسیم می شوند :
- عوارض الکتریکی قلبی که شامل آریتمی های طنی و فوق بطنی و بلوک هاست.
- عوارض مکانیکی قلبی که شامل ایجاد آنوریسم و پارگی و نارسایی قلبی است.
- عوارض خارج قلبی که شامل آمبولی مغزی پریکاردیت و سندرم درسلر است.
- عوارض الکتریکی قلبی
- عوارض مکانیکی قلب
- عوارض خارج قلبی
آریتمی ها : شایع ترین آریتمی به دنبال انفارکتوس میوکارد ، PVC است و خطرناک ترین آنها فیبریلاسیون بطنی (VF) و تاکی کاردی بطنی (V-Tach) است که می تواند منجر به مرگ بیمار شود.
فیبریلاسیون بطنی به دو صورت دیده می شود :
- در ۴ تا ۶ ساعت اول بعد از انفارکتوس ، به دلیل تحریک عصب واگ و برادی کاردی
- در ۲ تا ۳ روز بعد از انفارکتوس به دلیل اختلالات الکترولیتی و شوک کاردیوژنیک
سایر دیس ریتمی های شایع به دنبال انفارکتوس میوکارد : عبارتند از
- برادی کاردی سینوسی
- تاکی کاردی سینوسی
- PAT
- فلوتر و فیبریلاسیون دهلیزی
- بلوک های گره AV
- بلوک های شاخه ای
نارسایی پمپ قلب : از نظر کلینیکی به چهار صورت مختلف ظاهر می شود :
- (۳۰-۴۰% بیماران) بیمار علایم احتقان ریه ندارد ، صدای سوم قلب شنیده نمی شود ، در ریه ها صدای رال وجود ندارد .
- (۳۰-۵۰%) صدای سوم قلب شنیده می شود ، در کمتر از نصف ریه ها صدای رال وجود دارد .
- (۵-۱۰% بیماران) صدای سوم قلب شنیده می شود ، در بیشتر از نصف ریه ها صدای رال وجود دارد . بیمار علایم ادم ریه را از خود نشان می دهد .
- (۱۰% بیماران) شدید ترین نوع نارسایی قلبی است و به صورت شوک کاردیوژنیک ظاهر می شود .
شوک کاردیوژنیک : بیمار زمانی دچار نارسایی قلبی می شود که ۲۵ – ۲۰ % از بطن چپ او دچار نکروز شده باشد ، و زمانی شوک کاردیوژنیک ایجاد می شود که حدود ۴۰% از بطن چپ وی نکروز شده باشد . بیمار مبتلا به شوک کاردیوژنیک باید یک یا چند علامت زیر را داشته باشد :
- فشار سیستولیک زیر ۹۰ میلی متر جیوه بوده، و یا نسبت به فشار خون اولیه ، ۳۰ میلی کمتر جیوه کاهش داشته باشد.
- فشار متوسط کمتر از ۷۰ میلی متر جیوه
- سردی انتهاها ، عرق سرد ، تغییر رنگ پوست
- اختلال حواس ، هذیان
- اولیگوری
- عدم پاسخ بیمار به درمان های معمول
- سیکل شوک کاردیوژنیک بدین صورت است که اختلال در جریان خون کرونر ، منجر به ایسکمی میوکارد و اختلال در انقباض عضله قلب می شود و بدین ترتیب قلب نارسا می گردد . به دنبال نارسایی قلب ، برون ده کاهش یافته ، فشار خون کم می شود و کاهش فشار خون مجددا اختلال شدیدتری را در جریان خون کرونر ایجاد می کند . این سیکل آنقدر ادامه می یابد تا نهایتا به مرگ می انجامد.
پارگی قلب : از روز دوم و سوم تا هفته ی دوم بعد از انفارکتوس میوکارد انتظار بروز این عارضه وجود دارد . پارگی قلب از عوارض خطرناک انفارکتوس ترانس مورال آنترسپتال است. تابلوی بالینی آن به صورت مرگ ناگهانی با ریتم جدایی الکترومکانیکال (EMD) است.
پارگی سپتوم بین بطنی یا VSD : در اثر نکروز سپتوم بین بطنی ایجاد می شود . علایم آن به صورت تند شدن ناگهانی ریت قلب ، تنگی نفس شدید ، و ادم پولمونر است . در سمع ناحیه LSB سوفل خشن شنیده می شود.
نارسایی دریچه میترال : این اختلال در ۵۰% از بیماران مبتلا به انفارکتوس میوکارد شایع بوده ، می تواند به علت اختلال در عضله پاپیلاری یا پارگی کوردها و عضله پاپیلر باشد.
آنوریسم بطن چپ : از عوارض شایع انفارکتوس قدامی است و با ایجاد آریتمی های بطنی غیرقابل کنترل مشخص می گردد . در مشاهده و لمس آپیکال نیز یک ناحیه با حرکت غیرطبیعی حس می شود.
آمبولی مغزی و CVA : در روزهای اول بعد از انفارکتوس ممکن است لخته ای از ناحیه انفارکته قلب کنده شود . به این لخته ترومبوس مورال گفته می شود . حرکت این لخته و جایگزین شدن آن در مغز می تواند موجب همی پلژی گردد.
پریکاردیت زودرس : این عارضه در انفارکتوس ترانس مورال دیده می شود . نکروز اپیکارد سبب التهاب پریکاردیت و تجمع مایع و فیبرین در فضای پریکارد می گردد . ممکن است در اثر چسبندگی لایه احشایی پریکارد به اپیکارد ، در سمع ، صدای Friction Rub شنیده شود.
پریکاردیت دیررس یا سندرم Dressler : سندرمی شبیه به پریکاردیت است و ۱۲ – ۲ هفته بعد از انفارکتوس رخ می دهد . این سندرم بوسیله درد پلورتیک قفسه سینه ، تب ، درد مفاصل ، درد عضلانی ، صدای مالش پریکارد ، لکوسیتوز ، آنمی و افزایش سدیمانتاسیون خون مشخص می گردد . به نظر می آید که این یک واکنش اتوایمیون باشد.
سندرم دست – شانه : ممکن است یک یا چند ماه بعد از انفارکتوس میوکارد ، بیمار دچار درد ، سفتی و محدودیت حرکت در مفاصل شانه و بازو شود . این عارضه بیشتر در بیمارانی دیده می شود که به مدت طولانی استراحت مطلق داشته اند . این سندرم توسط فیزیوتراپی درمان می شود.
- برونر سودارث قلب و عروق و خون ( ویرایش یازدهم ۲۰۰۸ )
ویرایش : صدیقه سالمی ( عضو هیئت علمی دانشگاه ایران )
ترجمه : ژاله محمد علیها ، صدیقه عاصمی ، حلیمه امینی ( اعضای هیات علمی دانشگاه علوم پزشکی ایران و تهران ) - emergency critical care pocket guide
- ECG Notes Interpretation and Management Guide Second Edition
- Rosen Emergency Medicine 2014
تهیه ، تنظیم و آماده سازی : مرضیه براهویی و صادق دهقانی زاده
 the nursing station ایستگاه پرستاری
the nursing station ایستگاه پرستاری





ممنون استفاده کردیم
با سلام و تشکر از مطالب بسیار مفیدتان بنده پزشک عمومی هستم .در صورت امکان اجازه دانلود داده یا لطفا ایمیل نمایید ویا سایتی با چنین مشخصات سراغ دارید اطلاع دهید.منتظر پاسخ شما هستم .با تشکر
سلام.
میشه فایل این مطلبو برام بفرستین؟ میخام واسه کنفرانس دادن پرینت بگیرم خیلی ممنون میشم ازتون
با سلام و سپاس فراوان از مطالب مقاله استفاده کردم در صورت امکان درخواست ایمیل فایل مقاله را داشتم.
با تشکر
لطفا اگه میشه مطلبو مربوط به MIرو برام ایمیل کنید. با تشکر
چقدر عالی هستید شما
هنوز هم از مرجع های خوب پرستاری هستید.
هنوز هم مطلبی رو بخوام مرور کنم یا اطلاعات کسب کنم برمیگردم اینجا